

|
|
|||||||
| «бгж«ѕ «бЏбгн… ж «б ёдн… яб г« нќ’ «бгж«ѕ «бЏбгн… ж «б ёдн… : «б—н«÷н« - «бЏбжг «бЎ»нЏ… ж«бЌн«… - «бЏбжг «бЁн“н«∆н… - «бедѕ”… «бгѕдн… - едѕ”… «бЎ—«∆ё - «бедѕ”… «бгня«днян… - «бедѕ”… «бяе—»«∆н… - «б ”нн— «бгЌ«”»н ж «бг«бн - ”нн— ж «ё ’«ѕ |
Ён Ќ«б жћжѕ √н гж«÷нЏ √ж —ѕжѕ
гхќ«бЁ… гд ё»б «б√Џ÷«Ѕ° нх—ћм «б≈»б«џ Џде« Ёж—р« »«” ќѕ«г √нёжд…
![]() ( ё—н— Џд г‘«—я… ”н∆… )° ж «бгжћжѕ… √”Ёб яб г‘«—я… .
( ё—н— Џд г‘«—я… ”н∆… )° ж «бгжћжѕ… √”Ёб яб г‘«—я… .
| ¬ќ— «бгж«÷нЏ |
|
бд—«ћЏ гЏ« »—д«гћ г«ѕ… «бЁн“н«Ѕ- »я«бж—н« 2015- Ќ’—н« Џбм гд ѕм «бћбЁ…
 |
|
|
√ѕж« «бгж÷жЏ | «дж«Џ Џ—÷ «бгж÷жЏ |
|
|
—ёг «бг‘«—я… : 1 | ||||
|
«б”б«г Џбняг ж —Ќг… «ббе
н—ћм гд «б√Џ÷«Ѕ «бг”«ег… Ён Ў—Ќ - √ ж «б«нћ«»…Џд -«б√”∆б… .... гЏ«‘— «бд«ћЌнд: ≈д гд гёжг« «бдћ«Ќ " √д дЌёё г»ѕ√ «б Џ«жд " . ё«б Џ«бм ((жу уЏу«жудхж« Џубум «бъ»ц—шц жу«б шуёъжум ))[«бг«∆ѕ…:2]
¬ќ— Џѕнб ‘«н» «бѕж— »бё«”г 2015-05-08 Ён 21:12.
|
||||

|
|
|
—ёг «бг‘«—я… : 2 | |||
|
«бЁн“н«Ѕ ё—√ »«бёбг ж бн” »«бЏнд «бгћ—ѕ… Ќ м ж ≈д яд Џбм ѕ—«н… »”ежб… «б г—нд
|
|||

|
|
|
—ёг «бг‘«—я… : 3 | |||
|
1 - Ён ћѕжб «б ёѕг г м дя » »жЁ—… √ж »“н«ѕ… »«бд”»… бћ“∆ «бг«Ѕ њ * «бг«Ѕ »“н«ѕ… ≈–« я«д «–« я«д «б√ћ”«г «бг Ё«Џб« гдЌб… Ён «бг«Ѕ («б Ё«Џб н г ѕ«ќб гЌбжб г«∆н) **** »«” Ћд«Ѕ Ё«Џб« «б√” —… ж«б≈г«е… - «бжЌѕ… 06 - ж Ёяя «бг«Ѕ «б√я”ћндн - «бжЌѕ… «б√жбм - |
|||

|
|
|
—ёг «бг‘«—я… : 4 | |||
|
г«ен «бЏб«ё… »нд ”—Џ… «б Ё«Џб ж ”—Џ… «ќ Ё«Ѕ ж ‘яб джЏ янгн«∆н њ
бняд «б Ё«Џб «б «бн : αA + βB → γC + δD ќб«б “гд dtнќ Ён «бджЏ «бянгн«∆н A ж нўе— «бджЏ «бянгн«∆н C. [A ] → [A] Ц d[A] :”—Џ… «ќ Ё«Ѕ «бджЏ A я » VA = -d[A]/dt [C] → [C] + d[C] : ”—Џ… ‘яб «бджЏ «бянгн«∆н C я » VC = d[C]/dt Џб«ё… ”—Џ… «б Ё«Џб гЏ ”—Џ… «б«ќ Ё«Ѕ √ж «б ‘яб : 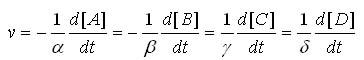 |
|||

|
|
|
—ёг «бг‘«—я… : 5 | |||
|
ггяд я «»… «бЏб«ё… «б”«»ё… »«бд”»… бЏѕѕ «бгжб« :
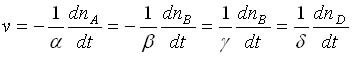 |
|||

|
|
|
—ёг «бг‘«—я… : 6 | |||
|
. «бЏб«ё… »нд «б ёѕг ж «б —ян“ «бгжбн .
бѕнд« «бЏб«ё… «б «бн… «б н нгяд «” д «ће«гд ћѕжб «б ёѕг :  »«бё”г… Џбм «бЌћг V дћѕ :  |
|||

|
|
|
—ёг «бг‘«—я… : 7 | |||
|
янЁ дЁ”— гће—н« «бЏ«гб «бЌ—ян бб Ё«Џб њ
нгяд бќн’ «б Ё”н— Ён «бгќЎЎ «б «бн : ѕ—ћ… «бЌ—«—… г— ЁЏ… => Џѕѕ «б ’«ѕг« «бЁЏ«б… г— ЁЏ- ж« — «б ’«ѕг« г— ЁЏ => Ё«Џб ”—нЏ - “ѕ«ѕ ”—Џ… «б Ё«Џб - жгде ѕ—ћ… «бЌ—«—… Џ«гб Ќ—ян —ян“ «бг Ё«Џб« г— ЁЏ => Џѕѕ «б ’«ѕг« г— ЁЏ - ’«ѕг «бЁЏ«б - => Ё«Џб ”—нЏ - “ѕ«ѕ ”—Џ… «б Ё«Џб - —ян“ «бг Ё«Џб« Џ«гб Ќ—ян |
|||

|
|
|
—ёг «бг‘«—я… : 8 | |||
|
|
|||

|
|
|
—ёг «бг‘«—я… : 9 | |||
|
√” «– «д« г«дн‘ Џ«—Ё… янЁ«‘ дя » гЏ«ѕб… «б«я”ѕ… «б≈—ћ«Џн… нЏдн г« дЏ—Ё‘ ‘яжд «бг«ѕ… бн дя »бе« гЏ«ѕб… б«я”ѕ… «Џе« ж «бг«ѕ… бн дя »бе« «б≈—ћ«Џ «Џе« ж«ббе Ќ«жб гн г«Ёег ‘
|
|||

|
|
|
—ёг «бг‘«—я… : 10 | |||
|
бгЏ—Ё… Џгбн… «б√я”ѕ… √ж ≈—ћ«Џ дё—√ гЏЎн« «б г—нд
ж дя » «б√дж«Џ «бянгн«∆н… «бг Ё«Џб… ж «б√дж«Џ «бянгн«∆н… «бд« ћ… . дЏнд «бджЏ Ён «бЋд«∆н… гƒя”ѕ / г—ћЏ ж дж«“д «бгЏ«ѕб… «бд’Ён… »ЌнЋ «–« я«д «б«бя —жд« Џбм «бнгнд Ё«бгЏ«ѕб… ен бб√я”ѕ… ж Ён «бн”«— Џѕ гЏ«ѕб… д’Ён… бб«—ћ«Џ ќб«’… : гд ќб«б гЏЎн« «б г—нд дЌѕѕ «бг Ё«Џб« гд «бдж« ћ ж дж«“д «бгЏ«ѕб… »« »«Џ «бќЎж« «б «бн… : 1 - гж«“д… «бЏд’— (џн— «б«я”ћнд ж«бенѕ—жћнд) 2- гж«“д… «б«я”ћнд »≈÷«Ё… Џѕѕ гЏнд гд ћ“н∆« «бг«Ѕ 3- гж«“д… бенѕ—жћнд »≈÷«Ё… Џѕѕ гЏнд гд ‘«—ѕ… «бенѕ—жћнд 4- гж«“д… «б‘Ќд« »«÷«Ё… Џѕѕ гЏнд гд «б«бя —жд« |
|||

|
|
|
—ёг «бг‘«—я… : 11 | |||
|
Ў»нё : Ё«Џб гЌбжб «б»—гдџ« «б»ж «”нжг гЏ гЌбжб «бг«Ѕ «б«жя”ћнд 1 ёг » Ќѕнѕ Ќѕѕ «бЋд«∆н« «бѕ«ќб… Ён «б Ё«Џб њ Џбг« √д «бг Ё«Џб« ен : MnO4- ж H2O2 2 - я «»… «бгЏ«ѕб нд «бд’Ён нд (ж«Ќѕ… √я”ѕ… ж«б√ќ—м »«б÷—ж—… ≈—ћ«Џ ).. MnO4- + 8H+ + 5e- = Mn2+ + 8H2O - б«Ќў «б«бя —жд« Ён «бг Ё«Џб« «–д Џгбн… ≈—ћ«Џ ж«б«бя —жд« Ён «бдж« ћ «–д √я”ѕ… H2O2 = 2H+ + 2e- + O2 дб«Ќў √д MnO4-Ён «бЎ—Ё «б–н Ёне «бя —жд« «–д еж гƒя”ѕ ж»«б «бн Mn2+ еж «бг—ћЏ Ё≈д «бЋд«∆н… (ox/red) ен (+MnO4-/Mn2) д »Џ дЁ” «бЎ—нё… «бЎ—нё… гЏ «бгЏ«ѕб… «бЋ«дн… H2O2 Ён «бЎ—Ё «б–н бн” Ёне «бя —жд« «–д еж г—ћЏ ж O2 гƒя”ѕ (O2/H2O2) |
|||

|
|
|
—ёг «бг‘«—я… : 12 | |||
|
«” «– Џдѕг« нЏЎжя гЏ«ѕб… «б«я”ѕ… «б«—ћ«Џн… |
|||

|
|
|
—ёг «бг‘«—я… : 13 | |||
|
хя » «б Ё«Џб« «бд’Ён… «бгж«Ёё… бЏгбн н «б√я”ѕ… ж«б≈—ћ«Џ° ж ж«“д гд ЌнЋ «б‘Ќд…
гЋ«б : -Cr (OH) 3 + IO3- ↔ I- + CrO42 хя » «б Ё«Џб« «бд’Ён… «бгж«Ёё… бЏгбн н «б√я”ѕ… ж«б≈—ћ«Џ° ж ж«“д гд ЌнЋ «б‘Ќд…: -Cr3+ → Cr6+ + 3e -I5+ +6e- → I √ж: -Cr (OH) 3 → CrO42- + 3e -IO3- + 6e- → I ж«“д –—… O Ён «б Ё«Џб «бд’Ён «б√жб: нхб«Ќў жћжѕ 4 –—« O Ён «бЎ—Ё «б√нгд° б–бя н÷«Ё ( 2OH-).4) ) ≈бм «бЎ—Ё «б√н”—° жЌнЋ нжћѕ -3OH √’б«р Ён «бг—я» Cr(OH)3 ° б–бя н÷«Ё ≈бм «бЎ—Ё «б√н”— -5OH ° жя–бя н÷«Ё 4H2O (»Џѕѕ –—« O ) ≈бм дЁ” «бЎ—Ё «б–н нЌжн –—« O ° √н: (Cr (OH) 3 + 5OH- ↔ CrO42- + 4H2O + 3e- (1 ж«“д –—… O Ён «б Ё«Џб «бд’Ён «бЋ«дн: нб«Ќў жћжѕ 3 –—« O Ён «бЎ—Ё «б√н”—° б–бя ÷«Ё (3.(-2OH)) ≈бм «бЎ—Ё «б√нгд жя–бя ÷«Ё 3H2O (»Џѕѕ –—« O ) ≈бм дЁ” «бЎ—Ё «б–н нЌжн –—« O ° √н: (IO3- + 6e- + 3H2O ↔ I- + 6OH- (2 нћЏб Џѕѕ «б«бя —жд« г ”«жн«р Ён «бгЏ«ѕб нд (1) ж (2)° ж–бя »÷—» «бгЏ«ѕб… (1) »«бгЏ«гб 2 ж÷—» «бгЏ«ѕб… (2) »«бгЏ«гб 1° ж»ћгЏ «бгЏ«ѕб нд «бћѕнѕ нд ж«б«ќ “«б: -2Cr (OH) 3 + 4OH- + IO3- ↔ 2CrO42- + 5H2O + I |
|||

|
|
|
—ёг «бг‘«—я… : 14 | |||
|
г—нд № ж«“д «б Ё«Џб« «б «бн… Ён ж”Ў Ќг÷н:
+SO32- + MnO4- ↔ SO42- + Mn2 Cr2O72- + H2S ↔ Cr3+ + S +C8H16O + Cr2O72- ↔ C8H14O + Cr3 1№ +SO32- + MnO4- ↔ SO42- + Mn2 -S(+4) ↔ S(+6) + 2e гж«“д… ‘Ќд… «бя»—н -SO32- ↔ SO42- + 2e (Mn(+7) + 5e- ↔ Mn(+2 гж«“д… ‘Ќд… «бгдџдн“ +MnO4- + 5e- ↔ Mn2 гж«“д… –—« O : SO32- +(1)H2O ↔ SO42- + (2)H+ + 2e- x5 MnO4- +(8)H+ + 4e- ↔ Mn2+ +(4)H2O x2 5SO32- +(5)H2O +2MnO4- +(16)H+ ↔ 52SO42- + (10)H+ + 2Mn2+ +(8)H2O 5SO32- + 2MnO4- +(6)H+ ↔ 52SO42- + 2Mn2+ +(3)H2O 2№ Cr2O72- + H2S ↔ Cr3+ + S хя » «б Ё«Џб« «бд’Ён… «бгж«Ёё… бЏгбн н «б√я”ѕ… ж«б≈—ћ«Џ ж ж« “д гд ЌнЋ «б‘Ќд…: +Cr2 (6+) + 6e- ↔ 2Cr3 гж«“д… ‘Ќд… «бя—жг -S2- ↔ S + 2e гж«“д… ‘Ќд… «бя»—н гж«“д… «бгЏ«ѕб… «бд’Ён… «б√жбм гд ЌнЋ «бг«ѕ…: +Cr2O72- +6e- ↔ 2Cr3 нхб«Ќў жћжѕ 7 –—« O Ён «бЎ—Ё «б√н”— ° б–бя нх÷«Ё 7H2O ≈бм «бЎ—Ё «б√нгд ж +14H ≈бм «бЎ—Ё «б√н”—: (Cr2O72- + 6e- + 14H+ ↔ 2Cr3+ + 7H2O (1 гж«“д… «бгЏ«ѕб… «бд’Ён… «бЋ«дн… гд ЌнЋ «бг«ѕ…: -H2S ↔ S + 2e нхб«Ќў жћжѕ –— н H Ён «бЎ—Ё «б√н”—° б–бя хж«“д H √жб«р »≈÷«Ё… +2H ≈бм «бЎ—Ё «б√нгд: (H2S ↔ S + 2H+ + 2e- (2 н”«жм Џѕѕ «б≈бя —жд« Ён «бгЏ«ѕб нд (1) ж(2) »÷—» «б√жбм »«бЏ«гб 1 ж«бЋ«дн… »«бЏ«гб 3° Ћг »«бћгЏ ж«б«ќ ’«—: Cr2O72- + 8H+ + 3H2S ↔ 2Cr3+ + 7H2O +3S 3№ +C8H16O + Cr2O72- ↔ C8H14O + Cr3 -C8(-14) ↔ C8(-12) + 2e гж«“д… ‘Ќд… «бя—»жд -C8H16O ↔ C8H14O + 2e (Cr2(+12) + 6e- ↔ 2Cr(+3 гж«“д… ‘Ќд… «бя—жг +Cr2O72- + 6e- ↔ 2 Cr3 гж«“д… –—« O : C8H16O ↔ C8H14O+(2)H+ + 2e- x3 Cr2O72- +(14)H+ + 6e- ↔ 2 Cr3+ +(7)H2O x1 3C8H16O + Cr2O72- +(14)H+ ↔ 3C8H14O+(6)H+ +2 Cr3+ +(7)H2O 3C8H16O + Cr2O72- +(8)H+ ↔ 3C8H14O +2 Cr3+ +(7)H2O г—нд № ж«“д Ё«Џб« «б√я”ѕ… ж«б≈—ћ«Џ «б «бн… Ён ж”Ў √”«”н: (Fe(CN)6]3- + N2H4(g) ↔ [Fe(CN)6]4- + N2(g] -Cr(OH)3 + ClO- ↔ CrO42- + Cl As2S3(s) + H2O2 ↔ AsO43- + SO42- + H2O -H2O2 + CrI3(s) ↔ CrO42- + IO4 -P4(s) + H2O ↔ PH3(g) + H2PO2 -Br2 ↔ Br- + BrO3 MnO4- + N2H4 ↔ MnO2 + N2 1№ (Fe(CN)6]3- + N2H4(g) ↔ [Fe(CN)6]4- + N2(g] (Fe(+3) + e- ↔ Fe(+2 гж«“д… ‘Ќд… «бЌѕнѕ -Fe(CN)6]3- + e- ↔ [Fe(CN)6]4] -N2(-4) ↔ N2(0) + 4e гж«“д… ‘Ќд… «б¬“ж -N2H4(g) ↔ N2(g) + 4e гж«“д… –—« H : N2H4(g) +(4)OH- ↔ N2(g) + (4)H2O + 4e- x1 Fe(CN)6]3- + e- ↔ [Fe(CN)6]4- x4] -N2H4(g) +(4)OH- +4[Fe(CN)6]3- ↔ N2(g) + (4)H2O + 4[Fe(CN)6]4 2№ -Cr(OH)3 + ClO- ↔ CrO42- + Cl -Cr(+3) ↔ Cr(+6) + 3e гж«“д… ‘Ќд… «бя—жг -Cr(OH)3 ↔ CrO42- + 3e (Cl(+1) + 2e- ↔ Cl(-1 гж«“д… ‘Ќд… «бябж— -ClO- + 2e- ↔ Cl гж«“д… –—« O : Cr(OH)3 +(5)OH- ↔ CrO42- + (4)H2O + 3e- x2 ClO- + H2O + 2e- ↔ Cl- +(2)OH- x3 -2Cr(OH)3 +(10)OH- + 3ClO- + 3H2O ↔ 2CrO42- + (8)H2O + 3Cl- +(6)OH -2Cr(OH)3 +(4)OH- + 3ClO- ↔ 2CrO42- + (5)H2O + 3Cl 3№ As2S3(s) + H2O2 ↔ AsO43- + SO42- + H2O -2As(+3) ↔ 2As(+5) + 4e гж«“д… ‘Ќд… «б“—днќ -S3(-2) ↔ 3S(+6) + 24e гж«“д… ‘Ќд… «бя»—н -As2S3(s) ↔ 2AsO43- + 3SO42- + 28e (O2(-1) + 2e- → 2O(-2 гж«“д… ‘Ќд… «б√я”ћнд H2O2 + 2e- ↔ 2H2O гж«“д… –—« O : As2S3(s) +(40)OH- ↔ 2AsO43- + 3SO42- + (20)H2O + 28e- x1 гж«“д… –—« H : -H2O2 + (2)H2O + 2e- ↔ 2H2O + (2)OH H2O2 + 2e- ↔ (2)OH- x14 -As2S3(s) +(40)OH- +14 H2O2 ↔ 2AsO43- + 3SO42- + (20)H2O +(28)OH As2S3(s) +(12)OH- +14 H2O2 ↔ 2AsO43- + 3SO42- + (20)H2O 4№ -H2O2 + CrI3(s) ↔ CrO42- + IO4 -Cr(+3) ↔ Cr(+6) + 3e гж«“д… ‘Ќд… «бя—жг -I3(-3) ↔ 3I(+7) + 24e гж«“д… ‘Ќд… «бнжѕ CrI3(s) ↔IO4- + 24e- -CrI3(s) ↔ CrO4- + 3IO4- + 27e гж«“д… –—« O : 3IO4↔ -CrI3(s) + (32)OH CrI3(s) + (32)OH- ↔ (16)H2O + 27e- + CrO42- + 3IO4- x2 H2O2 + 2e- ↔ (2)OH- x27 -2CrI3(s) + 10OH- + 27H2O2 ↔ 32H2O + 2CrO42- + 6IO4 5№ -P4(s) + H2O ↔ PH3(g) + H2PO2 -P4(0) ↔ 4P(+1) + 4e гж«“д… ‘Ќд… «бЁж”Ёж— -P4(S) ↔ 4H2PO2- + 4e P4(0) + 12e- D 4P(-3) гж«“д… ‘Ќд… «бЁж”Ёж— P4(S) + 12e- ↔ 4PH3(g) x1 P4(S) ↔ 4H2PO2- + 4e- x3 -4P4(S) ↔ 4PH3(g)+12H2PO2 гж«“д… –—« O : 4P4(S) +(48) OH- ↔4PH3(g)+12H2PO2- +(24) H2O гж«“д… –—« H : -4P4(S) + (48)OH- + (36) H2O ↔ 4PH3(g)+12H2PO2- +(24)H2O+ (36) OH -4P4(S) + (12)OH- +(12)H2O ↔ 4PH3(g) + 12H2PO2 6№ -Br2 ↔ Br- + BrO3 (Br2(0) + 2e- ↔ 2Br(-1 гж«“д… ‘Ќд… «б»—жг Br2 + 2e- ↔ 2Br- x5 -Br2(0) ↔ 2Br(+5) + 10e гж«“д… ‘Ќд… «б»—жг -Br2 ↔ 2BrO3- + 10e гж«“д… –—« O : Br2 + (12)OH- ↔ 2BrO3- +(6)H2O + 10e- x1 5Br2 + Br2 + (12)OH- ↔ 10Br- + 2BrO3- +(6)H2O 7№ MnO4- + N2H4 ↔ MnO2 + N2 хя » «б Ё«Џб« «бд’Ён… «бгж«Ёё… бЏгбн н «б√я”ѕ… ж«б≈—ћ«Џ ж ж« “д гд ЌнЋ «б‘Ќд…: +Mn7+ +3e- ↔ Mn4 -N24- ↔ N20 + 4e √ж: MnO4- +3e- ↔ MnO2 -N2H4 ↔ N2 + 4e хж«“д –—… O Ён «б Ё«Џб «бд’Ён «б√жб: нхб«Ќў жћжѕ –— нд ≈÷«Ён нд гд O Ён «бЎ—Ё «б√н”—° б–бя нх÷«Ё [2.(-2OH)] ≈бм «бЎ—Ё «б√нгд° Ћг нх÷«Ё 2H2O ≈бм дЁ” «бЎ—Ё «б–н нЌжн –—« O √н: (MnO4- +3e- + 2H2O ↔ MnO2 + 4OH- (1 хж«“д –—… H Ён «б Ё«Џб «бд’Ён «бЋ«дн: нхб«Ќў жћжѕ 4 –—« H Ён «бЎ—Ё «б√н”—° б–бя нх÷«Ё 4H2O ≈бм «бЎ—Ё «б√нгд жгд Ћг нх÷«Ё -4OH ≈бм «бЎ—Ё «б√н”—. (N2H4 + 4OH- ↔ N2 + 4e- + 4H2O (2 бћЏб Џѕѕ «б«бя —жд« г ”«жн Ён «бгЏ«ѕб нд (1) ж(2)° х÷—» «бгЏ«ѕб…(1) »«бЏ«гб 4 ж «бгЏ«ѕб… (2) »«бЏ«гб 3° ж»«бћгЏ ж«б«ќ ’«—: 4MnO4- + 3N2H4 ↔ 4MnO2 + 4OH- + 3N2 + 4H2O |
|||

|
|
|
—ёг «бг‘«—я… : 15 | |||
|
1)- √–я— «бёж«днд «б«дЌЁ«ў Ён «б Ё«Џб« «бджжн…
2)- √ягб «б Ё«Џб« «б «бн… :     |
|||

|
 |
| «бябг« «бѕб«бн… (Tags) |
| 2015-, г«ѕ…, гд ѕм, «бћбЁ…, «бЁн“н«Ѕ-, «д—«ћЏ, »я«бж—н«, Ќ’—н« |
| √ѕж« «бгж÷жЏ | |
| «дж«Џ Џ—÷ «бгж÷жЏ | |
|
|
«бг‘«—я« «бгд‘ж—… Џ»— Џд жће… дў— ’«Ќ»е« ЁёЎ° жб« хЏ»ш— »√н ‘яб гд «б√‘я«б Џд жће… дў— ≈ѕ«—… «бгд ѕм
«бгд ѕм џн— г”ƒжб Џд √н ≈ Ё«ё ћ«—н »нд «б√Џ÷«Ѕ... ЁЏбм «бћгнЏ Ќгшб «бг”ƒжбн…
Powered by vBulletin .Copyright © 2018 vBulletin Solutions, Inc